Nyhetsbrev
Missa inga nyheter! Anmäl dig till vårt nyhetsbrev som kommer en gång i månaden. Du som är medlem och har anmält din e-postadress får automatiskt nyhetsbrevet.

Kopplingen mellan modern hjärnforskning och Parkinsons sjukdom är ett av de mest livliga och kliniskt viktiga forskningsfälten inom neurovetenskap. Sjukdomen belyser både hjärnans sårbarhet och de stora vetenskapliga utmaningar som forskningen fortfarande står inför.
Den kanske mest grundläggande upptäckten inom Parkinsonforskningen gjordes redan på 1950–60-talet: sjukdomen orsakas av en kraftig brist på signalsubstansen dopamin. Forskare kunde då visa att de nervceller som producerar dopamin dör i ett specifikt område i mellanhjärnan, substantia nigra – den ”svarta substansen”.

Bilden visar en synaps – den punkt där nervceller kommunicerar genom kemiska signaler. Vid Parkinsons sjukdom påverkas denna signalöverföring när dopaminet, en av hjärnans viktigaste neurotransmittorer, gradvis minskar.
Dopaminet som dessa celler normalt skickar vidare till de basala ganglierna är avgörande för att starta, styra och finjustera kroppens rörelser. När dopamincellerna långsamt försvinner rubbas hela detta system, vilket leder till de typiska motoriska symtomen som skakningar, stelhet och långsamma rörelser.
Upptäckten banade också väg för utvecklingen av levodopa (L-dopa), som fortfarande är den mest effektiva symtomlindrande behandlingen. L-dopa kan passera blod–hjärnbarriären och omvandlas till dopamin inne i hjärnan – ett genombrott som dramatiskt förbättrade livet för många patienter.
På cellnivå har forskningen upptäckt något mycket karakteristiskt: sjuka nervceller innehåller onormala proteinrika inlagringar, så kallade Lewykroppar. Huvudkomponenten är proteinet alfasynuklein. I dag fokuserar en stor del av forskningsfältet på att förstå hur detta protein felveckas, klumpar ihop sig och sprids vidare från cell till cell – nästan på ett prionliknande sätt.
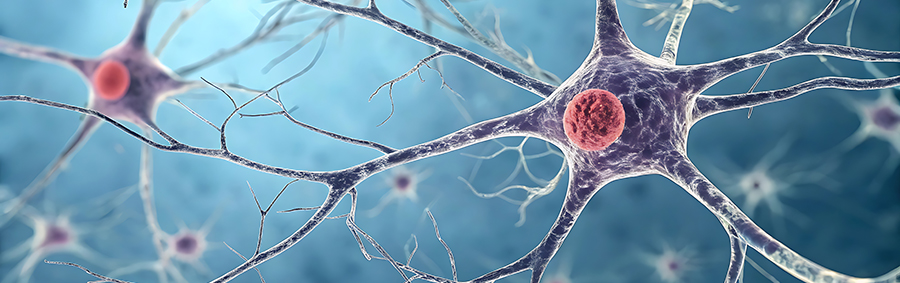
Vid Parkinsons sjukdom påverkas nätverk av nervceller när alfasynuklein börjar ansamlas i cellerna.
Denna spridningsteori kan förklara varför sjukdomen långsamt rör sig genom hjärnan och varför många icke-motoriska symtom, som sömnstörningar, depression eller kognitiva besvär, ofta kommer långt före motoriken.
Dagens Parkinsonforskning är bred och försöker angripa sjukdomen från flera håll samtidigt. Forskningen rör sig nu från enbart symtomlindring till att försöka påverka själva sjukdomsförloppet.
Tidig diagnos – att upptäcka sjukdomen innan den märks
Ett stort mål är att kunna diagnosticera Parkinsons sjukdom innan motoriska symtom uppstår. Här utvecklas avancerade avbildningstekniker, exempelvis PET-kameror med spårämnen som binder till dopamin eller till felveckat alfasynuklein. Med sådana metoder hoppas man kunna visualisera förändringar i hjärnan på ett mycket tidigt stadium.

Avancerad hjärnavbildning, en viktig metod för att tidigt upptäcka förändringar kopplade till Parkinsons sjukdom.
Parallellt studeras icke-motoriska symtom allt mer som möjliga ”varningssignaler” – till exempel sömnstörningar, depression eller kognitiv påverkan – som kan spegla att sjukdomen spridit sig till andra signalsystem än dopamin.
Celltransplantationer – att ersätta dopamincellerna
Ett av de mest lovande spåren är att ersätta de förlorade dopamincellerna med nya. Här ligger Sverige i framkant. Vid Lunds universitet har forskare lyckats ta fram stamceller som kan utvecklas till dopaminproducerande nervceller. Dessa kan transplanteras in i hjärnan för att ersätta de celler som gått förlorade.
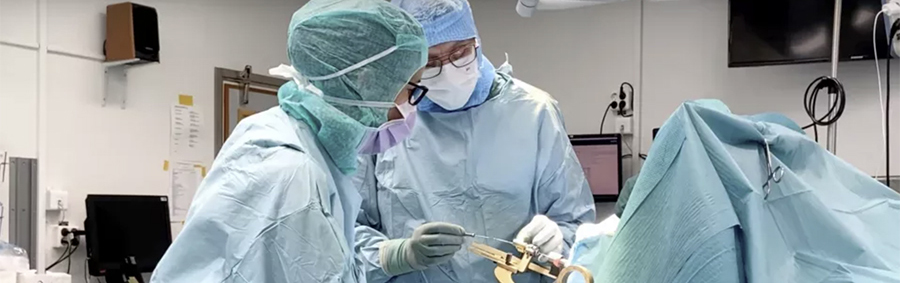 Bild från stamcellstransplantation. Foto: Skånes universitetssjukhus.
Bild från stamcellstransplantation. Foto: Skånes universitetssjukhus.
Kliniska försök, bland annat STEM-PD, pågår och har hittills visat god säkerhet och stabila resultat på gruppnivå. Förhoppningen är att denna typ av behandling på sikt ska kunna ge mer långvarig symtomlindring eller till och med påverka sjukdomens förlopp.
Neuromodulering – när elektricitet hjälper hjärnan
Djup hjärnstimulering (Deep Brain Stimulation, DBS) är en annan modern behandlingsmetod som växt fram ur hjärnforskningen. Genom att operera in tunna elektroder i specifika kärnor, oftast nucleus subthalamicus, går det att stabilisera de störda signalflöden som bidrar till symtomen.

Djup hjärnstimulering (DBS), en neurokirurgisk procedur där elektroder opereras in i specifika områden i hjärnan för att sända elektriska signaler.
För många patienter med långt framskriden sjukdom kan DBS ge en påtaglig förbättring av rörelseförmåga och vardagsfunktion, särskilt när läkemedelsbehandlingen inte längre räcker till eller ger för kraftiga biverkningar.
Inflammationens roll – astrocyter i fokus
Nya forskningsrön pekar allt tydligare på att neuroinflammation kan spela en viktig roll i sjukdomens förlopp. Här studeras bland annat astrocyter, hjärnans stora stödjeceller, som verkar förändras tidigt vid Parkinsons sjukdom.
Att dämpa eller modulera den inflammatoriska processen är ett växande forskningsspår. Om man bättre förstår hur immunsystemet i hjärnan bidrar till nervcellernas skada kan detta leda till framtida sjukdomsbromsande behandlingar.
Hjärnforskningen har under de senaste decennierna gått från att enbart lindra symtom till att aktivt försöka förstå och påverka sjukdomens grundläggande mekanismer. Målet är inte längre enbart bättre läkemedel, utan även möjligheten att bromsa eller till och med stoppa sjukdomsutvecklingen genom att angripa dopamincellernas sårbarhet, felveckningsprocessen eller inflammationen i hjärnan.
Thomas Winberg, Artikelförfattare
Maria Gyllström, Redigering och publicering
![]()
Kandel, E. R., Koester, J. D., Mack, S. H., & Siegelbaum, S. A. (2021). Principles of Neural Science (6:e uppl.). McGraw-Hill.
Bear, M. F., Connors, B. W., & Paradiso, M. A. (2020). Neuroscience: Exploring the Brain (5:e uppl.). Wolters Kluwer.
Purves, D. et al. (2018). Neuroscience (6:e uppl.). Oxford University Press.
Obeso, J. A., Stamelou, M., Goetz, C. G., et al. (2017). Past, present, and future of Parkinson’s disease. Movement Disorders, 32(9), 1264–1310.
Bloem, B. R., Okun, M. S., & Klein, C. (2021). Parkinson’s disease. The Lancet, 397, 2284–2303.
Surmeier, D. J., Obeso, J. A., & Halliday, G. M. (2017). Selective neuronal vulnerability in Parkinson disease. Nature Reviews Neuroscience, 18, 101–113.
Doidge, N. (2007). The Brain That Changes Itself. Viking Penguin.
Merzenich, M. M. (2013). Soft-Wired. Parnassus Publishing.
Kleim, J. A., & Jones, T. A. (2008). Principles of experience-dependent neural plasticity. Journal of Speech, Language, and Hearing Research, 51, S225–S239.
PubMed – https://pubmed.ncbi.nlm.nih.gov
National Institute of Neurological Disorders and Stroke (NINDS) – https://www.ninds.nih.gov
European Academy of Neurology (EAN) – https://www.ean.org
Karolinska Institutet, Institutionen för neurovetenskap – https://ki.se/neurovetenskap









